
GMP 인증
GMP(Good Manufacturing Practice)란?
식품 의약품의 안정성과 유효성을 품질면에서 보증하는 기본조건으로서 우수식품, 의약품의 제조 및 품질관리의 기준입니다.
의료기기의 설계, 개발, 제조, 시판 후 관리 등 전과정에 대한 품질시스템을 확보하여 안전하고, 유효하며, 의도된 용도에 적합한 품질의 제품을 일관성 있게 생산하는 것을 목적으로 합니다
GMP 적용범위
의료기기 제조, 수입 및 품질관리기준의 적용을 받는 범위는 다음과 같습니다.
1. 제조 또는 수입허가를 받거나 신고하고자 하는 자
▷ 품목허가(신고)전에 적합성 평가를 신청하여 인정받을 수 있도록 함
2. 임상시험용 의료기기를 제조 또는 수입하고자 하는 자
▷ 의료기기법 시행규칙 제13조제1항제10호에 규정
3. 적합성평가를 받고자 하는 의료기기 제조업자 또는 수입업자
▷ 품목허가후 판매 전에 적합인정을 받을 수 있도록 함
4. 품질관리심사 업무를 하고자 하는 자
*적합성 인정 등 심사의 제외사항
수출만을 목적으로 제조, 수입하는 의료기기 또는 1등급 의료기기는 GMP 심사 제외 대상이나, 수출국가의 요구사항, 품질관리 목적 등의 사유인 경우 적합성인정 등 심사를 받을 수 있습니다.
GMP 심사구분
최초심사 : 제조업자 또는 수입업자가 해당 제조소에 대하여 의료기기 GMP를 최초로 신청하는 경우
추가심사 : 다른 품목군의 의료기기를 추가하는 경우
변경심사 : 제조소 소재지를 변경하는 경우 (단,제품의 품질과 관계가 적은 보관소 시험실의 변경 또는 혁신의료기기소프트웨어 제조소의 소제지 변경은 제외)
정기갱신심사 : 고시에 의하여 3년마다 1회 받아야 하는 정기적인 심사
의료기기 정의 및 등급분류
1. 의료기기란
사람이나 동물에게 단독 또는 조합하여 사용되는 기구, 기계, 장치, 재료 또는 이와 유사한 제품으로서 사용목적과 사용 시 인체에 미치는 잠재적 위해성의 정도에 따라 4개의 등급으로 분류됨
2. 의료기기 등급
1등급 : 잠재적 위험성이 거의 없는 의료기기
2등급: 잠재적 위험성이 낮은 의료기기
3등급 : 중증도의 잠재적 위해성을 가진 의료기기
4등급 : 고도의 위해성을 가진 의료기기
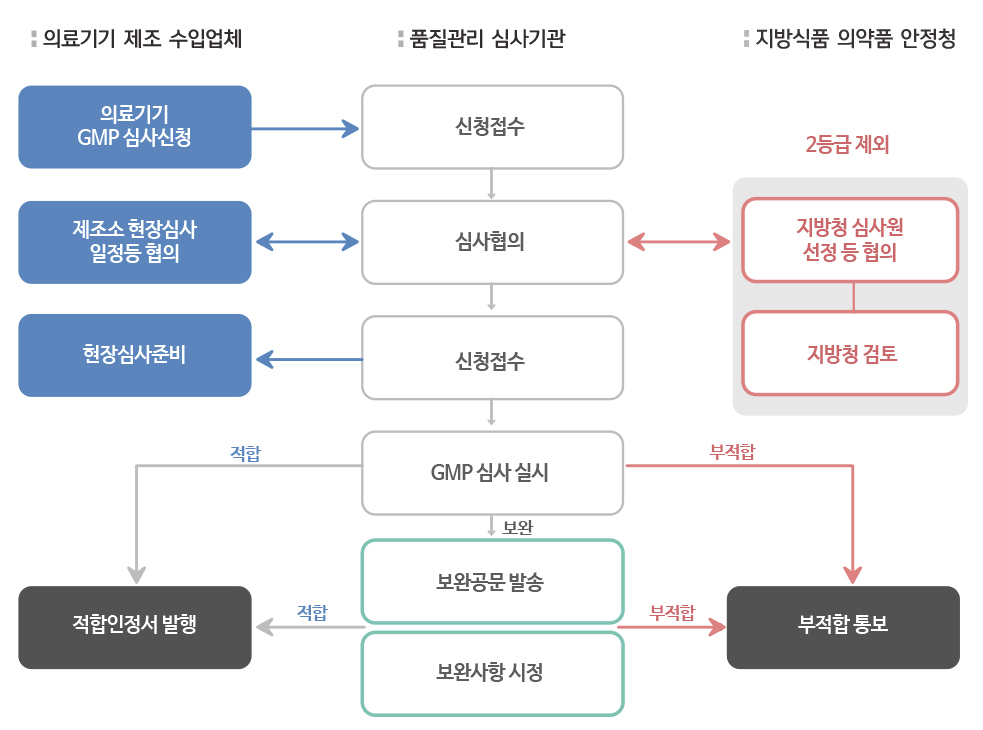
GMP 인증절차
적합성평가 신청 제출서류
신청서
· 수입(제조)허가증 사본
· 제조소 개요
· 제조품질관련 종업원수
· 의료기기 목록(품목명, 등급)
· 생산국 품질경영시스템 적합인증서 사본
· 제조소 시설개요
· 소재지 및 업무범위
· 타기관 실사자료(해당하는 경우)
· 품질매뉴얼
· 제품표준서
· 설치 또는 사후지원이 필요한 제품은 관련 설명서
의료기기 품질책임자
1. 의료기기 품질책임자 지정 의무화
: 법률 개정[14.1.28]에 따라 일정 자격의 품질책임자 지정 의무화
2. 의료기기 품질책임자 자격요조건 (6가지 중 하나만 만족하면 됨)
– 안경사, 치과위생사, 방사선사 등 면허 소지자
– 의공기사, 품질경영기사 자격 취득자
– 의료기기 관련 전공 학사 보유자
– 의료기기 관련 전공 아닌 학사 보유자 + 품질관리 경력 1년 이상
– 전문대졸 등 + 품질관리 경력 3년 이상
– 고졸 + 품질관리 경력 5년 이상
GMP인증 빠른 상담문의


